MENDELEVYUM |
|
Temel özellikleri |
|
| Atom numarası | 101 |
| Element serisi | Aktinitler |
| Grup, periyot, blok | -, 7, f |
| Görünüş | bilinmiyor |
| Atom ağırlığı | 258 g/mol |
| Elektron dizilimi | [Rn] 5f13 7s2 |
| Enerji seviyesi başına Elektronlar |
2, 8, 18, 32, 31, 8, 2 |
| CAS kayıt numarası | 7440-11-1 |
| Fiziksel Özellikleri | |
| Maddenin hâli | katı |
| Sıvı hâldeki yoğunluğu | g/cm³ |
| Ergime noktası | 1100 °K 827 °C |
| Kaynama noktası | °K °C |
| Ergime ısısı | kJ/mol |
| Buharlaşma ısısı | kJ/mol |
| Atom özellikleri | |
| Kristal yapısı | |
| Yükseltgenme seviyeleri | 2, 3 |
| Elektronegatifliği | 1.3 Pauling ölçeği |
| İyonlaşma enerjisi | 635 kJ/mol |
| Atom yarıçapı | pm |
| Atom yarıçapı (hes.) | pm |
| Kovalent yarıçapı | pm |
| Van der Waals yarıçapı | pm |
| Diğer özellikleri | |
| Elektrik direnci | nΩ·m (20°C’de) |
| Isıl iletkenlik | W/(m·K) |
| Isıl genleşme | µm/(m·K) (25°C’de) |
| Ses hızı | m/s (‘de) |
| Mohs sertliği | |
| Vickers sertliği | MPa |
| Brinell sertliği | MPa |
Mendelevyum a, sentetik elemanı ile sembolü Kırmızı ( eski Mv ) ve atom numarası 101 metalik bir radyoaktif olarak transuranik elemanı aktinit serileri, şu anda boyunca makroskopik miktarlarda üretilebilen olamaz atom sayısına göre birinci eleman olan nötron hafif elementlerdendır. Üçüncü-son aktinid ve dokuzuncu transuranik elementtir. Sadece partikül hızlandırıcılarda daha hafif elementleri yüklü partiküller ile bombardıman ederek üretilebilir. Toplam on yedi mendelevium izotopu bilinmektedir, en kararlı olanı 51 günlük yarılanma ömrü ile 258 Md ; bununla birlikte, daha kısa ömürlü 256 Md (yarı ömür 1.17 saat), daha büyük ölçekte üretilebildiği için kimyada en yaygın olarak kullanılır.
Mendelevyum bombardıman tarafından keşfedilen aynştaynyum ile alfa parçacıklarının 1955, aynı yöntem günümüzde üretmek için kullanılan. Kimyasal elementlerin periyodik tablosunun babası Dmitri Mendeleev’in adı verilmiştir. İzotop einsteinium-253’ün mevcut mikrogram miktarları kullanılarak, her saat bir milyondan fazla mendeleviyum atomu üretilebilir. Mendeleviumun kimyası, +3 oksidasyon durumunun üstünlüğü ve aynı zamanda erişilebilir +2 oksidasyon durumu ile geç aktinidler için tipiktir. Mendeleviyumun bilinen tüm izotopları nispeten kısa yarı ömürlere sahiptir; şu anda temel bilimsel araştırma dışında kullanımı yoktur ve sadece küçük miktarlar üretilmektedir.
KEŞİF

Ağustos 1939’da Berkeley , California Üniversitesi Lawrence Radyasyon Laboratuvarı’nda ki 60 inçlik siklotron
Ekip, mendelevium üretiminin mümkün olup olmayacağını tahmin etmek için kaba bir hesaplama yaptı. Üretilecek atom sayısı, hedef malzemenin atom sayısı, hedefin enine kesiti, iyon ışını yoğunluğu ve bombardıman süresinin çarpımına yaklaşık olarak eşit olacaktır; bu son faktör, yarı ömrü sırasına göre bir süre bombardıman sırasında ürünün yarı ömrü ile ilgiliydi. Bu, deney başına bir atom verdi. Bu nedenle optimum koşullar altında, deney başına yalnızca bir 101 element atomunun hazırlanması beklenebilir. Bu hesaplama, deneye devam etmenin mümkün olduğunu gösterdi. [4] Hedef malzeme, einsteinium-253, ışınlanan plütonyumdan kolayca üretilebilir: bir yıllık ışınlama bir milyar atom verirdi ve üç haftalık yarı ömrü, element 101 deneylerinin, üretilen einsteinyum ayrılıp saflaştırıldıktan sonra bir hafta içinde yapılabileceği anlamına geliyordu. Bununla birlikte, 10 gerekli olan yoğunluğunun elde edilmesi için bir siklotron yükseltmek için gerekli olan 14 saniyede alfa parçacıkları; Seaborg gerekli fonlar için başvurdu. [5]

Mendelevium’un keşfini kanıtlayan kalem izi ve notları gösteren veri sayfası.
İlk deneyler Eylül 1954’te yapıldı. Mendelevium atomlarında alfa bozunması görülmedi; bu nedenle Ghiorso, mendeleviyumun elektron yakalama ile fermiyuma bozunduğunu ve bunun yerine kendiliğinden fisyon olaylarını aramak için deneyin tekrarlanması gerektiğini öne sürdü . [5] Deneyin tekrarı Şubat 1955’te gerçekleşti. [5]

Öğe, Dmitri Mendeleev’in adını aldı .
ÖZELLİKLER
FİZİKSEL
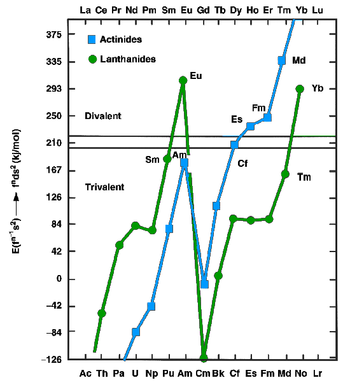
F-blok lantanitler ve aktinitler için bir f elektronunu d alt kabuğuna yükseltmek için gereken enerji. Yaklaşık 210 kJ / mol’ün üzerinde, bu enerji, üç değerlikli halin daha büyük kristal enerjisi tarafından sağlanamayacak kadar yüksektir ve bu nedenle einsteinium, fermium, mendelevium, lantanid öropiyum ve iterbiyum gibi iki değerli metalleri oluşturur . (Nobelium’un da iki değerlikli bir metal oluşturması beklenmektedir, ancak bu henüz doğrulanmamıştır.) [11]
Metalik haldeki lantanitler ve aktinitler, iki değerlikli (öropiyum ve iterbiyum gibi) veya üç değerlikli (diğer lantanitlerin çoğu) metaller olarak var olabilir. İlki fn s2 konfigürasyonuna sahipken, ikincisi f n −1 d1 s2 konfigürasyonuna sahiptir. 1975 yılında, Johansson ve Rosengren, hem iki değerlikli hem de üç değerlikli metaller olarak metal lantanitlerin ve aktinitlerin kohezif enerjileri (kristalleşme entalpileri) için ölçülen ve tahmin edilen değerleri inceledi.[13][14] Sonuç olarak, mendelevium için [Rn] 5f 13 7s 2 konfigürasyonu üzerindeki [Rn] 5f12 6d1 7s2 konfigürasyonunun artan bağlanma enerjisinin, bir 5f elektronunu 6d’ye yükseltmek için gereken enerjiyi telafi etmek için yeterli olmadığıdır. Çok geç aktinidler için de geçerlidir: bu nedenle einsteinium, fermium, mendelevium ve nobelium’un divalent metaller olması bekleniyordu. [13] Aktinid serisinin sonuçlanmasından çok önce iki değerlikli durumun artan baskınlığı, artan atom sayısı ile artan 5f elektronlarının göreli stabilizasyonuna atfedilir.[15] Thermochromatographic 1976 ile 1982 Zvara ve Hübener ile mendelevyum eser miktarlarda çalışmalar bu tahmini teyit etmiştir. [12] 1990’da, Haire ve Gibson, mendelevium metalinin 134 ile 142 kJ/mol arasındabir süblimasyon entalpisine sahip olduğunu tahmin ettiler. [12] Divalent mendelevium metalin metalik yarıçapı yaklaşık 194 ± 10 pm tarihinde.[12] Diğer iki değerlikli geç aktinitler gibi (bir kez daha üç değerlikli lavrensiyum hariç), metalik mendeleviyum yüz merkezli bir kübik kristal yapı almalıdır.[1] Mendelevium’un erime noktası, komşu element nobelium için öngörülen değerle aynı olan 827 ° C olarak tahmin edildi. [16] Yoğunluğunun yaklaşık olduğu tahmin ediliyor 10.3 ± 0.7 g / cm 3. [1]
KİMYASAL
Mendeleviumun kimyası çoğunlukla sadece +3 veya +2 oksidasyon durumlarını alabildiği solüsyonda bilinir. +1 durumu da bildirildi, ancak henüz onaylanmadı. [17]
Mendelevium’un keşfinden önce Seaborg ve Katz, sulu çözeltide ağırlıklı olarak üç değerlikli olması gerektiğini ve dolayısıyla diğer tripozitif lantanidlere ve aktinitlere benzer şekilde davranması gerektiğini öngördü. 1955 yılında mendelevium sentezinden sonra, bu tahminler ilk olarak, reçinenin bir katyon değişim kolonundan üç değerlikli aktinid elüsyon sekansındaki fermiyumdan hemen sonra ayrıştırıldığının keşfinde ve daha sonra mendeleviumun oluşabileceğine dair 1967 gözleminde doğrulanmıştır. Üç değerlikli lantanit tuzları ile birlikte çökeltilen çözünmez hidroksitler ve florürler. [17]Katyon değişimi ve çözücü ekstraksiyon çalışmaları, mendeleviyumun, önceki aktinit olan fermiyumdan biraz daha küçük bir iyonik yarıçapa sahip üç değerlikli bir aktinid olduğu sonucuna götürdü.[17] Mendelevium, 1,2-sikloheksandinitrilotetraasetik asit (DCTA) ile koordinasyon kompleksleri oluşturabilir . [17]
Olarak indirgeme koşulları, mendelevyum (III) kolayca sulu çözelti içinde stabil olan mendelevyum (II) ‘e azaltılabilir. [17] Standart indirgeme potansiyeli arasında E ° (Md3+ → Kırmızı2+ 🙂 çift çeşitli -0.10 V veya -0.20 V 1967 yılında tahmin edilen [17] , daha sonra 2013, deney değeri kurulan -0.16 ± 0.05 H. [18] Buna karşılık, E ° (Md 3+ → Md 0) 1,74 V civarında olmalı ve E ° (Md2+ → Md0) −2,5 V civarında olmalıdır. [17] Mendelevium (II) ‘s elüsyon davranışı, stronsiyum (II) ve öropiyum (II) ile karşılaştırılmıştır. [17]
1973 yılında, mendeleviumun daha yüksek oksidasyon durumlarını samaryum (II) ile azaltarak elde eden Rus bilim adamları tarafından mendelevium (I) üretildiği bildirildi. Bu nötr su içerisinde kararlı olduğu bulunmuştur etanol çözeltisi ve olmak homolog için sezyum (I). Bununla birlikte, daha sonraki deneyler, mendelevium (I) için hiçbir kanıt bulamadı ve mendeleviyumun, tek değerlikli alkali metaller gibi değil, indirgendiğinde divalent elementler gibi davrandığını buldu.[17] Yine de, Rus ekibi mendeleviyumun alkali metal klorürlerle birlikte kristalize edilmesinin termodinamiği üzerine daha fazla araştırma yaptı.ve mendeleviumun (I) iki değerlikli elementlerle karışık kristaller oluşturduğu ve böylece onlarla birlikte kristalleştiği sonucuna vardı. +1 oksidasyon durumunun durumu hala belirsizdir. [17]
E° (Md4+→Md3+) 1975 yılında +5,4 V olarak tahmin edilmiş olmasına rağmen, mendeleviumun (III) mendelevium’a (IV) oksitlenebileceğini düşündürse de, güçlü oksitleyici madde sodyum bizmutat ile 1967 deneyleri oksitlenemedi. mendelevium (III) ila mendelevium (IV). [17]
ATOMİK
Bir mendelevium atomunun 101 elektronu vardır ve bunlardan en az üçü (ve belki de dördü) değerlik elektronları olarak hareket edebilir. [Rn] 5f13 7s2 (temel durum terim sembolü 2 F 7/2) konfigürasyonunda düzenlenmeleri beklenmektedir, ancak bu elektron konfigürasyonunun deneysel doğrulaması 2006 yılı itibarıyla henüz yapılmamıştır. [19] Bileşikleri oluşturmada, üç valans elektronu kaybedilebilir ve geride bir [Rn] 5f 12 çekirdeği bırakılabilir ve bu, üçlü pozitif durumda [Rn] 5f n elektron konfigürasyonları ile diğer aktinitler tarafından belirlenen eğilime uygundur. İlk iyonlaşma potansiyeli mendeleviumun en fazla (6.58 ± 0.07) eV olduğu, 7s elektronlarının 5f olanlardan önce iyonize olacağı varsayımına dayanılarak 1974 yılında ölçüldü. [20] Bu değer, mendelevium’un kıtlığı ve yüksek radyoaktivite nedeniyle o zamandan beri henüz daha fazla rafine edilmemiştir.[21] Heksoordinat Md 3+ iyonik yarıçapının ilk olarak 1978’de 91.2 pm civarında olduğu tahmin edilmişti; [17] Dağılım katsayıları ve iyonik yarıçap arasındaki logaritmik eğilime dayalı 1988 hesaplamaları 89.6 pm’lik bir değer ve ayrıca hidrasyon entalpisi üretti .−3654 ± 12 kJ / mol . [17] Md 2+ , 115 pm’lik bir iyonik yarıçapa ve 1413 kJ / mol hidrasyon entalpisine sahip olmalıdır; Md + , 117 pm iyonik yarıçapa sahip olmalıdır. [17]
İZOTOPLAR
Kütle numaraları 244 ile 260 arasında değişen on yedi mendelevium izotopu bilinmektedir; hepsi radyoaktif. [22] Ayrıca, beş çekirdek izomerler bilinmektedir: 245 Md, 247m Md, 249m Md, 254m Kırmızı ve 258m Md. [3] [23] Bunlardan, en uzun ömürlü bir izotop olan 258 Kırmızı bir yarı ömürle 51.5 gün ve en uzun ömürlü izomer, 58.0 dakikalık yarılanma ömrü ile 258m Md’dir . [3] [23] Bununla birlikte, daha kısa ömürlü 256Md (yarılanma ömrü 1.17 saat), kimyasal deneylerde daha sık kullanılır, çünkü einsteinyumun alfa parçacık ışınlamasından daha büyük miktarlarda üretilebilir. [22] sonra 258 Md, ikinci en dayanıklı mendelevyum izotopları 260 Kırmızı 31.8 günlük bir yarı ömürle, 257 5,52 saatlik bir yarılanma ömrü ile Kırmızı 259 1.60 saatlik bir yarılanma ömrü ile Kırmızı ve 256 Kırmızı 1.17 saatlik yarılanma ömrü iledir. Geri kalan tüm mendelevium izotoplarının yarı ömürleri bir saatten azdır ve bunların çoğunun yarı ömürleri 5 dakikadan azdır. [3] [22] [23]
Mendelevium izotoplarının yarı ömürleri çoğunlukla 244 Md’den itibaren sorunsuz bir şekilde artarak 258 Md’de maksimuma ulaşır. [3][22][23] Deneyler ve tahminler, yarı ömürlerin 260 Md’den ayrı olarak azalacağını göstermektedir. 31.8 günlük yarı ömür, [3] [22] [23], uzun ömürlü çekirdeklerin göreceli kararlılık adasına bir sınır oluşturan protonların karşılıklı itilmesinden dolayı, kendiliğinden fisyon baskın bozunma modu [3] haline gelirken [3] Aktinitlerde serisi. [24]
Mendeleviumun kimyasal olarak en önemli izotopu olan Mendelevium-256, zamanın% 90’ında elektron yakalaması ve % 10’unda alfa bozunması yoluyla bozulur. [22] En kolay şekilde elektron yakalama kızı fermium-256’nın kendiliğinden bölünmesiyle tespit edilir, ancak kendiliğinden bölünmeye uğrayan diğer çekirdeklerin varlığında mendelevium-256 (7.205 ve 7.139 MeV) için karakteristik enerjilerde alfa bozunur daha kullanışlı tanımlama sağlar. [25]
ÜRETİM VE İZOLASYON
En hafif mendelevium izotopları (244Md ile 247 Md) çoğunlukla bizmut hedeflerin ağır argon iyonları ile bombardımanı yoluyla üretilirken, biraz daha ağır olanlar ( 248 Md ila 253 Md) plütonyum ve amerikum hedeflerinin daha hafif karbon ve nitrojen iyonlarıyla bombardıman edilmesiyle üretilir. En önemli ve en kararlı izotoplar, 254 Md ila 258 Md aralığındadır ve alfa parçacıkları ile einsteinium izotoplarının bombardımanı yoluyla üretilir ve einsteinium-253, -254 ve -255’in tümü kullanılabilir. 259Kırmızı bir şekilde üretilir kızı arasında 259, No ve 260 Kırmızı bir üretilebilir transfer reaksiyonu aynştaynyum-254 arasında oksijen-18. [22] Tipik olarak, en yaygın kullanılan izotop 256 Md, einsteinium-253 veya -254’ü alfa parçacıklarıyla bombardıman ederek üretilir: Einsteinium-254, daha uzun bir yarı ömre sahip olduğundan ve bu nedenle bir hedef olarak kullanılabildiğinden, mevcut olduğunda tercih edilir. daha uzun süre. [22] Mevcut mikrogram miktarlarda einsteinium kullanılarak, femtogram miktarlarında mendelevium-256 üretilebilir. [22]
Üretilen mendelevium-256 atomlarının geri tepme momentumu, onları üretildikleri einsteinium hedefinden fiziksel olarak uzağa getirmek için kullanılır ve onları , hemen arkasındaki ince bir metal folyoya (genellikle berilyum, alüminyum, platin veya altın) getirir. [25] Bu, hem maliyetli olan hem de pahalı einsteinium hedefinin yeniden kullanılmasını önleyen acil kimyasal ayırma ihtiyacını ortadan kaldırır. [25] Mendelevium atomları daha sonra bir gaz atmosferinde (sıklıkla helyum ) tutulur ve reaksiyon odasındaki küçük bir açıklıktan çıkan bir gaz jeti mendelevyumu birlikte taşır. [25]Uzun bir kılcal tüp kullanılarak ve helyum gazına potasyum klorür aerosolleri dahil edilerek, mendeleviyum atomları kimyasal olarak analiz edilmek ve miktarları belirlenmek üzere onlarca metreden fazla taşınabilmektedir . [7] [25] mendelevyum bundan sonra folyo malzemesi ve diğer ayrılabilir fizyon ürünleri daha sonra folyo üzerine asit tatbik etmek ve ile eş çökeltme ile mendelevyum lantan flüorür bundan sonra bir, katyon değişim % 10 reçine sütunu etanol doymuş çözeltisi bir eluant görevi gören hidroklorik asit ile. Bununla birlikte, folyo altından yapılmışsa ve yeterince ince ise, anyon değişim kromatografisi kullanarak üç değerlikli aktinitleri altından ayırmadan önce altını aqua regia’da çözmek yeterlidir, eluant 6 M hidroklorik asittir. [25]
Mendelevium, son olarak, bir katyon değişim reçinesi kolonundan seçici elüsyon kullanılarak diğer üç değerlikli aktinitlerden ayrılabilir ki elüan, amonyak a-HIB’dir. [25] Gaz püskürtme yöntemini kullanmak genellikle ilk iki adımı gereksiz kılar.[25] Yukarıdaki prosedür, transeinsteinium elementlerin ayrılması için en yaygın kullanılan prosedürdür. [25]
Üç değerlikli aktinitleri ayırmanın başka bir olası yolu, sabit organik faz olarak bis- (2-etilheksil) fosforik asit (HDEHP olarak kısaltılır) ve mobil sulu faz olarak nitrik asit kullanılarak çözücü ekstraksiyon kromatografisidir. Aktinid elüsyon sekansı, daha ağır aktinidlerin daha sonra ayrıştırılması için katyon değişim reçinesi kolonununkinden tersine çevrilir. Bu yöntemle ayrılan mendeleviyum, reçine kolonuna kıyasla organik kompleks yapıcı madde içermeme avantajına sahiptir ve dezavantaj, mendeleviyumun fermiyumdan sonra elüsyon dizisinde çok geç ayrıştırılmasıdır. [7] [25]
Mendelevium’u izole etmek için başka bir yöntem, Md2+‘nın Es 3+ ve Fm 3+ özelliklerinden farklı elüsyon özelliklerini kullanır. İlk adımlar yukarıdaki ile aynıdır ve özütleme kromatografisi için HDEHP’yi kullanır, ancak mendelevyumu lantan florür yerine terbiyum florür ile birlikte çökeltir. Daha sonra mendelevyuma 50 mg krom ilave edilerek 0.1 M hidroklorik asitte çinko veya cıva ile +2 durumuna indirgenir. [25] Çözücü ekstraksiyonu daha sonra devam eder ve üç değerlikli ve dört değerli lantanitler ve aktinitler kolon üzerinde kalırken mendelevyum (II) hidroklorik asit içinde kalmaz ve kalmaz. Daha sonra kullanılarak +3 durumuna yeniden oksitlenirhidrojen peroksit ve daha sonra 2 M hidroklorik asit (krom dahil safsızlıkları gidermek için) ve son olarak 6 M hidroklorik asit (mendelevyumu çıkarmak için) ile seçici elüsyon yoluyla izole edilir. [25] Elüsyon maddesi olarak 1 M hidroklorik asit kullanarak, alkali toprak metalleri gibi davrandığı yerde Md (III) ‘ü Md (II)’ ye indirgeyen bir katyonit ve çinko amalgam kolonunu kullanmak da mümkündür.[25] Termokromatografik kimyasal izolasyon, uçucu mendeleviyum heksafloroasetilasetonat kullanılarak sağlanabilir ve benzer fermiyum bileşiği de bilinmektedir ve aynı zamanda uçucudur. [25]
TOKSİTETE
Çok az kişi mendelevium ile temas etse de, Uluslararası Radyolojik Koruma Komisyonu en kararlı izotop için yıllık maruz kalma sınırları belirlemiştir. Mendelevyum-258 için, yutma limiti 9 x 10 ayarlandı 5 becquerels (1 Bq saniyede bir çürüme eşdeğerdir) ve 6000 Bq soluma sınırıdır. [26]
KAYNAKÇA
KAYNAKLAR
|

