NOBELYUM |
| Temel özellikleri | |
| Atom numarası | 102 |
| Element serisi | Aktinitler |
| Grup, periyot, blok | Grup yok, 7. Dönem, F Bloğu |
| Görünüş | |
| Atom ağırlığı | g/mol |
| Elektron dizilimi | Rn 5f14 7s2 |
| Enerji seviyesi başına Elektronlar |
2, 8, 18, 32, 32, 8, 2 |
| CAS kayıt numarası | 10028-14-5 |
| Fiziksel Özellikleri | |
| Maddenin hâli | katı |
| Sıvı hâldeki yoğunluğu | ? g/cm³ |
| Ergime noktası | 1100 °K 827 °C |
| Kaynama noktası | °K °C |
| Ergime ısısı | kJ/mol |
| Buharlaşma ısısı | kJ/mol |
| Atom özellikleri | |
| Kristal yapısı | |
| Yükseltgenme seviyeleri | |
| Elektronegatifliği | 1.3 Pauling ölçeği |
| İyonlaşma enerjisi | 642 kJ/mol |
| Atom yarıçapı | pm |
| Atom yarıçapı (hes.) | pm |
| Kovalent yarıçapı | pm |
| Van der Waals yarıçapı | pm |
| Diğer özellikleri | |
| Elektrik direnci | nΩ·m (20°C’de) |
| Isıl iletkenlik | W/(m·K) |
| Isıl genleşme | µm/(m·K) (25°C’de) |
| Ses hızı | m/s (‘de) |
| Mohs sertliği | |
| Vickers sertliği | MPa |
| Brinell sertliği | MPa |
Nobelyum, amerikyum veya küriyumdan elde edilen yapay element. 1957’de Nobel fizik enstitüsü tarafından bulunmuştur.
Nobelium bir olan sentetik kimyasal element ile sembol yoktur ve atom numarası 102’dir. Dinamitin mucidi ve bilimsel gelişime teşviki nedeniyle Alfred Nobel anısıyla adlandırılmıştır. Transuranik elemanı ve sondan bir önceki üyesidir aktinid serisindendir. Atom numarası 100’ün üzerinde olan tüm elementler gibi nobelium da sadece daha hafif elementleri yüklü partiküller ile bombardıman ederek partikül hızlandırıcılarda üretilebilir. Toplam on iki nobelium izotopunun var olduğu bilinmektedir; en kararlı 259 Bir ile hiçbir yarılanma ömrü 58 dakika, ama daha kısa ömürlü 255 o büyük ölçekte üretilebilir çünkü Hayır (yarılanma ömrü 3.1 dakika) en sık kimyada kullanılır.
Kimya deneyleri daha ağır olarak bu nobelium davranır doğruladı homologundan için iterbiyum periyodik tabloda. Nobelium’un kimyasal özellikleri tam olarak bilinmemektedir: çoğunlukla sadece sulu çözeltide bilinirler. Nobelium’un keşfinden önce, kararlı bir +2 oksidasyon durumu ve diğer aktinitlerin +3 durum karakteristiğini göstereceği tahmin ediliyordu: Bu tahminler daha sonra doğrulandı, çünkü +2 durumu +3 durumundan çok daha kararlı. içerisinde sulu çözelti ve +3 halde nobelyum tutmak zordur.
1950’lerde ve 1960’larda, İsveç, Sovyetler Birliği ve Amerika Birleşik Devletleri’ndeki laboratuarlarda nobelium keşfine dair birçok iddia yapıldı. İsveçli bilim adamları kısa süre sonra iddialarını geri çekmiş olsalar da, keşfin önceliği ve dolayısıyla elementin isimlendirilmesi Sovyet ve Amerikalı bilim adamları arasında tartışmalıydı ve 1997 yılına kadar Uluslararası Saf ve Uygulamalı Kimya Birliği (IUPAC) Sovyetler’e kredi vermedi. Ekip keşfi ile birlikte, ancak literatürde uzun süredir kullanılması nedeniyle elementin adı olarak İsveç’in önerisi olan nobelium’u korudu.
GİRİŞ

Bir nükleer füzyon reaksiyonunun grafik tasviri . İki çekirdek, bir nötron yayarak birleşir . Bu ana kadar yeni elementler yaratan reaksiyonlar benzerdi, tek olası fark, birkaç tekil nötronun bazen serbest kalması veya hiç salınmamasıydı.
Işın hedefin içinden geçer ve bir sonraki bölme olan ayırıcıya ulaşır; yeni bir çekirdek üretilirse bu ışın ile taşınır. [17] Ayırıcıda, yeni üretilen çekirdek diğer çekirdeklerden (orijinal ışınınki ve diğer reaksiyon ürünlerinden) ayrılır [e] ve çekirdeği durduran bir yüzey bariyeri dedektörüne aktarılır . Dedektör üzerindeki yaklaşan etkinin tam konumu işaretlenmiştir; enerji ve varış zamanı da işaretlenmiştir. [17] Aktarım yaklaşık 10-6 saniye sürüyor; tespit edilebilmesi için çekirdeğin bu kadar uzun süre hayatta kalması gerekir.[20] Çekirdek, bozunması ve konumu, enerjisi kaydedildikten sonra tekrar kaydedilir.ve çürümenin zamanı ölçülür. [17]
Bir çekirdeğin kararlılığı, güçlü etkileşim ile sağlanır. Ancak menzili çok kısadır; çekirdekler büyüdükçe, en dıştakinükleonlar (protonlar ve nötronlar) üzerindeki etkisi zayıflar. Aynı zamanda çekirdek, sınırsız menzile sahip olduğu için protonlar arasındaki elektrostatik itme ile parçalanır. [21] En ağır elementlerin çekirdekleri bu nedenle teorik olarak tahmin edilir [22] ve şimdiye kadar [23] bu tür itmenin neden olduğu bozunma modları yoluyla esas olarak bozulduğu gözlemlenmiştir: alfa bozunması ve kendiliğinden fisyon; [f] bu modlar, süper ağır elementlerin çekirdekleri için baskındır. Alfa bozunmaları, yayılan alfa parçacıkları tarafından kaydedilir ve bozunma ürünlerinin gerçek bozulmadan önce belirlenmesi kolaydır; eğer böyle bir bozulma veya bir dizi ardışık bozunma bilinen bir çekirdek üretirse, bir reaksiyonun orijinal ürünü aritmetik olarak belirlenebilir. [g] Kendiliğinden fisyon, ürün olarak çeşitli çekirdekler üretir, bu nedenle orijinal çekirdek kızlarından belirlenemez. [h]
En ağır unsurlardan birini sentezlemeyi amaçlayan fizikçilerin elindeki bilgiler, bu nedenle detektörlerde toplanan bilgilerdir: bir parçacığın detektöre varış yeri, enerjisi ve zamanı ve bozunması. Fizikçiler bu verileri analiz ediyorlar ve gerçekten de yeni bir elementten kaynaklandığı ve iddia edilenden farklı bir çekirdekten kaynaklanamayacağı sonucuna varmaya çalışıyorlar. Genellikle, sağlanan veriler yeni bir öğenin kesinlikle yaratıldığı sonucuna varmak için yetersizdir ve gözlemlenen etkiler için başka bir açıklama yoktur ve verilerin yorumlanmasında hatalar yapılmıştır.
KEŞİF

Öğe, Alfred Nobel’in adını almıştır .
102. elementin keşfinin ilk duyurusu 1957’de İsveç’teki Nobel Enstitüsünde fizikçiler tarafından duyuruldu . Ekip , yarım saatlik aralıklarla yirmi beş saat boyunca karbon-13 iyonlarıyla bir küriyum hedefini bombaladıklarını bildirdi. Bombardımanlar arasında, hedefe iyon değişim kimyası yapıldı. Elli bombardımandan on ikisi, fermiyum (atom numarası Z = 100) ve kaliforniyumdan (Z = 98) daha önce ayrıştırılan damlalar halinde olan (8.5 ± 0.1) MeV alfa parçacıkları yayan numuneler içeriyordu. Yarılanma süresi bildirilen 10 dakika idi ve 251 102 veya 253 102’ye atandı, ancak gözlemlenen alfa parçacıklarının , 102 öğesinin elektron yakalamasından yaratılan muhtemelen kısa ömürlü bir mendelevium (Z = 101) izotopundan olma olasılığı hariç tutulmadı. [30] takım ismi önerilmiştir nobelyum, yeni elemanı (Resim) [31] [32] hemen IUPAC tarafından onaylandı olan [33] Dubna grubu acele olarak 1968 yılında, özelliği bir karar. [34] Ertesi yıl, Lawrence Berkeley Ulusal Laboratuvarı’ndaki bilim adamlarıdeneyi tekrarladı ancak arka plan etkisi olmayan herhangi bir 8.5 MeV olayı bulamadı. [30]
1959’da İsveç ekibi, Berkeley ekibinin 102. elementi 1958’de tespit edemediğini, keşfettiklerini iddia ederek açıklamaya çalıştı. Ancak daha sonraki çalışmaları hiçbir nobelium daha hafif izotoplar göstermiştir 259 İsveçli takımın sonuçları en muhtemel olduğu 3 dakikadan fazla var bir yarılanma ömrü ile No (hayır daha ağır izotoplar İsveçli deneylerde üretilen olabilirdi) ve toryum -225 yarı ömrü 8 dakikadır ve hızlı bir şekilde üçlü alfa bozunmasına uğrayarak polonyuma dönüşür8.53612 MeV bozunma enerjisine sahip -213. Bu hipotez, kullanılan reaksiyonda toryum-225’in kolaylıkla üretilebilmesi ve kullanılan kimyasal yöntemlerle ayrılmayacağı gerçeğiyle ağırlık vermektedir. Daha sonra nobelium üzerinde yapılan çalışmalar, iki değerlikli durumun üç değerlikli olandan daha kararlı olduğunu ve dolayısıyla iki değerlikli nobelium diğer üç değerlikli aktinitlerle ayrışmayacağından, alfa parçacıklarını yayan numunelerin nobelium içermediğini gösterdi. [30] Böylece, İsveç ekibi daha sonra iddialarını geri çekti ve faaliyeti arka plan efektleriyle ilişkilendirdi. [33]
Albert Ghiorso , Glenn T. Seaborg, John R. Walton ve Torbjørn Sikkeland’dan oluşan Berkeley ekibi, 1958’de 102 elementinin sentezini talep etti. Ekip, bir curium hedefini bombalamak için yeni ağır iyon lineer hızlandırıcıyı (HILAC) kullandı. (% 95 244 Cm ve % 5 246 Cm) 13 C ve 12 C iyonları ile. Bunlar İsveçlilerce talep 8.5 MeV aktivitesi onaylayamadık yerine, fermium-250 sözde kızı yapısını ve özelliklerini tespit etmek mümkün 254, belirgin bir vardı (küriyum-246 tarafından üretilmiştir) 102 yarı ömrüarasında ~ 3 sn. Daha sonra 1963 Dubna çalışması, 254102’nin bu reaksiyonda üretilebileceğini doğruladı, ancak yarı ömrünün aslında 50 ± 10 sn. 1967’de Berkeley ekibi, bulunan izotopun gerçekten 250 Fm olduğunu, ancak gerçekte ilişkili olan izotopun, 252 102’nin torunu olan kaliforniyum -244 olduğunu belirterek çalışmalarını savunmaya çalıştı. 244. Enerji farklılıkları daha sonra “çözülme ve sürüklenme sorunlarına” atfedildi, ancak bunlar daha önce rapor edilmemişti ve diğer sonuçları da etkilemiş olmalıydı. 1977 deneyleri, 252 102’nin gerçekten de 2,3 saniyelik bir yarı ömre sahip olduğunu gösterdi. Bununla birlikte, 1973 çalışması, 250 Fm geri tepmesinin de izomerik geçişten kolayca üretilebileceğini gösterdi .250m Fm (yarılanma ömrü 1.8 s) olan, kullanılan enerjide reaksiyonda da oluşmuş olabilir. [30] Buna göre, bu deneyde gerçekte hiçbir nobelium üretilmemiş olması muhtemeldir. [30]
1959’da ekip çalışmalarına devam etti ve ağırlıklı olarak 8.3 MeV alfa parçacığının emisyonu ile bozulan bir izotop üretebildiklerini iddia etti, yarı ömrü 3 saniye ve ilişkili % 30 spontan fisyon dalı ile Aktivite başlangıçta 254 102 olarak atandı, ancak daha sonra 252 102 olarak değiştirildi. Ancak, aynı zamanda, zor koşullar nedeniyle nobelyum üretildiğinin kesin olmadığını da belirttiler. [30] Berkeley ekibi element için İsveç ekibinin önerilen adı olan “nobelium” u benimsemeye karar verdi. [33]
- 24496Santimetre + 126C → 256102Hayır* → 252102Hayır + 4 10n
Bu arada Dubna’da, 102. elementi de sentezlemek amacıyla 1958 ve 1960’da deneyler yapıldı. İlk 1958 deney bombardımana plütonyum-239 ve -241 ile oksijen-16 iyonları. Enerjileri 8.5 MeV’nin biraz üzerinde olan bazı alfa bozunmaları gözlemlendi ve 251,252,253 102’ye atandı, ancak ekip kurşun veya bizmut safsızlıklarından (nobelium üretmeyecek olan) izotop oluşumunun göz ardı edilemeyeceğini yazdı. Daha sonraki 1958 deneyleri cıva, talyumdan yeni izotopların üretilebileceğini belirtirken, kurşun veya bizmut safsızlıkları, bilim adamları, 30 saniyenin altında bir yarı ömür ve (8.8 ± 0.5) MeV’lik bir bozunma enerjisinden bahsederek, 102 elementinin bu reaksiyondan üretilebileceği sonucuna hala sahiptiler. Daha sonra 1960 deneyleri bunların arka plan etkileri olduğunu kanıtladı. 1967 deneyleri de bozunma enerjisini (8.6 ± 0.4) MeV’ye düşürdü, ancak her iki değer de muhtemelen 253 Hayır veya 254 No. [30] ile eşleşmek için çok yüksek. [30] Dubna ekibi daha sonra 1970’te ve yine 1987’de bu sonuçların kesin değil. [30]
1961’de Berkeley bilim adamları , kaliforniyumun bor ve karbon iyonları ile reaksiyonunda 103 elementinin keşfini iddia ettiler . İzotop 257 103’ün üretimini iddia ettiler ve ayrıca yarı ömrü 15 saniye ve alfa bozunma enerjisi 8.2 MeV olan 102 elementinin alfa bozunan izotopunu sentezlediklerini iddia ettiler. Görev için bir neden belirtmeden bunu 255102’ye atadılar. Değerler şu anda 255 Hayır olarak bilinenlerle uyuşmaz ancak şu anda 257 Hayır olarak bilinenlerle aynı fikirde olsalar da, bu izotop muhtemelen bu deneyde rol oynasa da keşfi sonuçsuz kaldı. [30]
Eleman 102 üzerindeki çalışmalar da Dubna’da devam etti ve 1964’te, bir uranyum-238 hedefinin neon iyonlarıyla reaksiyonundan element 102’yi sentezleyerek element 102 izotoplarının alfa bozunum kızlarını tespit etmek için deneyler yapıldı . Ürünler bir gümüş tutucu folyo boyunca taşındı ve kimyasal olarak saflaştırıldı ve 250 Fm ve 252 Fm izotopları tespit edildi. 252 Fm verimi, ebeveyn 256102’nin de sentezlendiğinin kanıtı olarak yorumlandı: 252 Fm’nin, bir alfa parçacığının fazla nötronlarla eşzamanlı emisyonu ile bu reaksiyonda doğrudan üretilebileceğine dikkat çekildi. emin olun252 Fm doğrudan alıcı folyoya gidemedi. 256 102 için tespit edilen yarı ömür 8 saniyeydi, bu daha modern 1967 değerinden (3,2±0,2) çok daha yüksektir. [30] 1966’da 254 102 için 243 Am (15N, 4n) 254 102 ve 238 U (22 Ne, 6n) 254 102 reaksiyonları kullanılarak (50 ± 10) s’lik bir yarı ömür bularak daha ileri deneyler yapıldı. : o sırada bu değer ile önceki Berkeley değeri arasındaki tutarsızlık anlaşılmamıştı, ancak daha sonraki çalışmalar 250m izomer oluşumunun kanıtlandığını kanıtladı. Dubna deneylerinde Fm, Berkeley deneylerinden daha az olasıydı. Geriye dönüp baktığımızda, 254 102’deki Dubna sonuçları muhtemelen doğruydu ve artık 102 öğesinin kesin tespiti olarak düşünülebilir. [30]
1966’da Dubna’dan çok ikna edici bir deney daha yayınlandı, yine aynı iki reaksiyon kullanılarak, 254 102’nin aslında Berkeley tarafından iddia edilen 3 saniyeden çok daha uzun bir yarı ömre sahip olduğu sonucuna varıldı. [30] 1967’de Berkeley’de ve 1971’de Oak Ridge Ulusal Laboratuvarı’nda yapılan sonraki çalışmalar, 102. elementin keşfini tam olarak doğruladı ve daha önceki gözlemleri açıklığa kavuşturdu. [33] Aralık 1966’da, Berkeley grubu Dubna deneylerini tekrarladı ve tam olarak onayladı ve bu verileri nihayet daha önce sentezledikleri ancak o sırada henüz tanımlayamadıkları izotopları doğru bir şekilde atamak için kullandı ve bu nedenle 1958’den 1961’e. [33]
- 23892U + 2210Ne → 260102Hayır* → 254102Hayır + 6 10n
1969’da Dubna ekibi, element 102 üzerinde kimyasal deneyler yaptı ve bunun iterbiyumun daha ağır homologu olarak davrandığı sonucuna vardı . Rus bilim adamları , yakın zamanda ölmüş olan Irène Joliot-Curie’den sonra yeni element için joliotium (Jo) adını önerdiler ve her grubun kendi önerdiği adlarını kullandığı birkaç on yıl boyunca çözülemeyecek bir adlandırma tartışması yarattı. [33]
1992’de, IUPAC – IUPAP Transfermium Çalışma Grubu (TWG) keşif iddialarını yeniden değerlendirdi ve yalnızca 1966’dan kalma Dubna çalışmasının doğru bir şekilde tespit ettiği ve o sırada 102 atom numaralı çekirdeklere bozunmaları atadığı sonucuna vardı. Dubna ekibi, bu nedenle, 1959’da Berkeley’de tespit edilmiş olması mümkün olsa da, resmi olarak nobelium’u keşfedenler olarak kabul edilmektedir. [30] Bu karar, ertesi yıl Berkeley tarafından 101’den 103’e Dubna, IUPAC’ın kararına katılırken “boş zaman kaybı”. [34]
1994 yılında, öğe adlandırma tartışmasına yönelik çözüm girişiminin bir parçası olarak, IUPAC 101-109 öğelerinin adları onayladı. 102. element için, Nobelium (Hayır) adını, literatüre 30 yıl içerisinde yerleştiği ve Alfred Nobel’in bu şekilde anılması gerektiği gerekçesiyle onayladı. [35] için, çoğunlukla kaşifleri seçimler saygı değil 1994 isim, üzerinde haykırış, bir yorum süresi izledi, ve 1995 IUPAC elemanı 102 adlı flerovyum ya sonra yeni bir öneri bir parçası olarak (Fİ) Giorgi Flyorov veya onun adını taşıyan Flerov Nükleer Reaksiyonlar Laboratuvarı. [36]Bu öneri de kabul edilmedi ve 1997’de nobelium adı geri getirildi. [35] Bugün aynı sembolle flerovium adı, element 114’ü ifade etmektedir . [37]
ÖZELLİKLER
FİZİKSEL
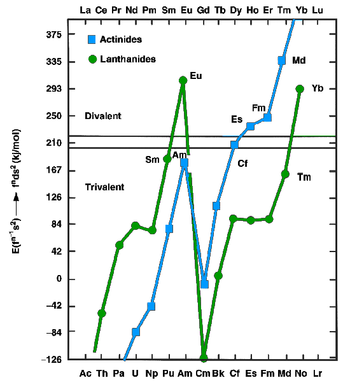
F-blok lantanitler ve aktinitler için bir f elektronunu d alt kabuğuna yükseltmek için gereken enerji. Yaklaşık 210 kJ / mol’ün üzerinde, bu enerji, üç değerlikli durumun daha büyük kristal enerjisi tarafından sağlanamayacak kadar yüksektir ve bu nedenle einsteinyum, fermiyum ve mendelevyum, lantanit öropyum ve iterbiyum gibi iki değerli metalleri oluşturur . Nobelium’un da iki değerlikli bir metal oluşturması bekleniyor, ancak bu henüz doğrulanmadı. [38]
Metalik haldeki lantanitler ve aktinitler, iki değerlikli (öropiyum ve iterbiyum gibi) veya üç değerlikli (diğer lantanitlerin çoğu) metaller olarak var olabilir. İlki fn s2 konfigürasyonuna sahipken, ikincisi fn −1 d1 s2 konfigürasyonuna sahiptir. 1975 yılında, Johansson ve Rosengren, hem iki değerlikli hem de üç değerlikli metaller olarak metal lantanitlerin ve aktinitlerin kohezif enerjileri (kristalleşme entalpileri) için ölçülen ve tahmin edilen değerleri inceledi.[40][41] Sonuç, nobelium için [Rn] 5f 14 7s 2 konfigürasyonuna göre [Rn] 5f 13 6d 1 7s 2 konfigürasyonunun artan bağlanma enerjisinin, bir 5f elektronunu 6d’ye yükseltmek için gereken enerjiyi telafi etmek için yeterli olmadığıdır. çok geç aktinidler için de geçerlidir: dolayısıyla einsteinium, fermium, mendelevium ve nobelium’un divalent metaller olması bekleniyordu, ancak nobelium için bu tahmin henüz doğrulanmadı.[40] Aktinid serisinin sonuçlanmasından çok önce iki değerlikli durumun artan baskınlığı, göreceliğe atfedilir. 5f elektronlarının stabilizasyonu, artan atom sayısı ile artar: Bunun bir etkisi, diğer tüm lantanidler ve aktinitlerin aksine nobelium’un üç değerlikli yerine ağırlıklı olarak iki değerlikli olmasıdır. [42] 1986’da, nobelium metalinin 126 kJ/mol arasında bir süblimasyon entalpisine sahip olduğu tahmin ediliyordu ki bu, einsteinyum, fermiyum ve mendelevyum değerlerine yakın bir değerdir ve nobeliumun iki değerli bir metal oluşturacağı teorisini destekler. [39] Diğer iki değerlikli geç aktinitler gibi (bir kez daha üç değerlikli lavrensiyum hariç), metalik nobelium yüz merkezli bir kübik kristal yapı almalıdır.[2] Divalent nobelium metal, yaklaşık 197 metalik yarı çapa sahip olmalıdır.[39] Nobelium’un erime noktasının, komşu element mendelevium için tahmin edilen değerle aynı olan 827 ° C olduğu tahmin edilmektedir. [43] Yoğunluğunun yaklaşık 9,9±0,4 g/cm 3 olduğu tahmin edilmektedir . [2]
KİMYASAL
Soyluyumun kimyası tam olarak karakterize edilmemiştir ve yalnızca +3 veya +2 oksidasyon durumlarını alabildiği sulu çözeltide bilinir, ikincisi daha kararlıdır. [31] Nobelium keşfedilmeden önce büyük ölçüde, çözümde diğer aktinidler gibi davranması bekleniyordu, üç değerlikli durum baskındı; ancak, Seaborg 1949’da +2 durumunun nobelium için nispeten kararlı olacağını tahmin etti, çünkü No 2+ iyon , kararlı dolgulu 5f 14 kabuk dahil olmak üzere temel elektron konfigürasyonuna [Rn] 5f 14 sahip olacaktı . Bu tahminin doğrulanması on dokuz yıl aldı. [44]
1967’de nobelium’un kimyasal davranışını terbiyum , kaliforniyum ve fermiyumunkiyle karşılaştırmak için deneyler yapıldı . Dört elementin tamamı klor ile reaksiyona sokuldu ve ortaya çıkan klorürler, bir gazla taşınan bir tüp boyunca biriktirildi. Üretilen nobelium klorürün katı yüzeyler üzerinde güçlü bir şekilde adsorbe edildiği bulundu ve bu da araştırılan diğer üç elementin klorürleri gibi çok uçucu olmadığını kanıtladı. Ancak, her iki NOCl 2 ve NOCl 3 uçucu olmayan bir davranış sergileyen beklenen ve bu nedenle bu deney nobelium tercih edilen oksidasyon durumu ne olduğu sonuç vermedi.[44] Nobelium’un +2 devletini desteklediğinin belirlenmesi, sonraki yıla kadar beklemek zorunda kaldı; katyon değişim kromatografisi ve birlikte çökeltme deneyleri, yaklaşık elli bin 255 Atom yok üzerinde yapıldı ve diğer aktinitlerden ve daha fazlasından farklı davrandığını buldu. iki değerli toprak alkali metaller gibi . Bu, sulu çözeltide nobeliumun, güçlü oksitleyiciler olmadığındaiki değerlikli durumda en kararlı olduğunu kanıtladı. [44] 1974’teki sonraki deneyler, nobeliumun Ca 2+ ve Sr 2+ arasında alkali toprak metallerle ayrıştırıldığını gösterdi. [44] Nobelium, sulu çözeltide +2 durumunun en yaygın ve kararlı olduğu bilinen tek f-blok elementidir. Bu, aktinid serisinin sonunda 5f ve 6d orbitalleri arasındaki büyük enerji boşluğu nedeniyle oluşur. [45]
7s alt kabuğunun relativistik stabilizasyonunun, nobelium dihydride, NoH 2’yi büyük ölçüde istikrarsızlaştırması ve 6d 3/2 spinor üzerinde 7p 1/2 spinorun relativistik stabilizasyonunun, nobelium atomlarındaki uyarılmış durumların yerine 7s ve 7p katkısı olduğu anlamına gelir. beklenen 6d katkı. NoH 2 molekülündeki uzun No – H mesafeleri ve önemli yük aktarımı , bu molekül için 5.94 D’ lik bir dipol momenti ile aşırı iyonikliğe yol açar . Bu molekülde, nobeliumun , özellikle n s 2 ile bir alkali toprak metal gibi davranarak, ana grup benzeri davranış sergilemesi beklenir.valans kabuğu konfigürasyonu ve çekirdek benzeri 5f orbitalleri. [46]
Nobelium’un klorür iyonlarıyla kompleks oluşturabilme yeteneği, oldukça zayıf bir şekilde komplekslenen baryumunkine çok benzer. [44] Sulu 0.5 M amonyum nitrat çözeltisi içinde sitrat, oksalat ve asetat ile kompleks oluşturabilme yeteneği, stronsiyumunkine biraz daha yakın olmasına rağmen kalsiyum ve stronsiyum arasındadır. [44]
Standart indirgeme potansiyeli arasında E ° (Resim 3+ → Resim 2+) çift 1,4 ila +1.5 olduğu 1967 yılında tahmin edilen V ; [44] daha sonra 2009’da sadece +0.75 V olarak bulundu. [47] Pozitif değer, No 2 + ‘ nın No 3 + ‘ dan daha stabil olduğunu ve No 3 + ‘ nın iyi bir oksitleyici ajan olduğunu gösterir. E ° (No 2+ → No0) ve E ° (No 3+→No0) için alıntılanan değerler kaynaklar arasında farklılık gösterse de, kabul edilen standart tahminler −2.61 ve −1.26 V. [44]Bu değer için tahmin edilmiştir E ° (Resim4+→Resim3+) bir çift +6.5 V olur [44] enerjileri Gibbs Resim için oluşum 3+ ve No 2 + -342 olduğu tahmin edilmektedir ve Sırasıyla −480 kJ / mol. [44]
ATOMİK
Bir nobelium atomunun 102 elektronu vardır ve bunlardan üçü değerlik elektronu olarak işlev görebilir. [Rn] 5f 14 7s 2 (temel durum terim sembolü 1 S0) konfigürasyonunda düzenlenmeleri beklenmektedir , ancak bu elektron konfigürasyonunun deneysel doğrulaması 2006 itibariyle henüz yapılmamıştır. [39] Bileşiklerin oluşturulmasında, tümü üç valans elektronu, geride bir [Rn] 5f 13 çekirdeği bırakarak kaybedilebilir: bu, üçlü pozitif durumda [Rn] 5f n elektron konfigürasyonları ile diğer aktinidler tarafından belirlenen eğilime uygundur. Yine de, sadece iki değerlik elektronunun kaybolması ve geride kararlı bir [Rn] 5f bırakması daha olasıdır 14dolu bir 5f 14 kabuk ile çekirdek. Nobelium’un ilk iyonlaşma potansiyeli, 7s elektronlarının 5f elektronlarından önce iyonize olacağı varsayımına dayanarak, 1974’te en fazla (6.65 ± 0.07) eV olarak ölçüldü; [48] Nobelium’un kıtlığı ve yüksek radyoaktivite nedeniyle bu değer henüz daha fazla rafine edilmemiştir. [49] Heksoordinat ve okta koordinat No 3+’nin iyonik yarıçapının önceleri 1978’de sırasıyla 90 ve 102 pm civarında olduğu tahmin edilmişti; [44] No 2 + ‘ nın iyonik yarıçapı deneysel olarak iki anlamlı rakama 100 pm olarak bulundu. [39] No 2+ hidrasyon entalpisi 1486 kJ/mol olarak hesaplanmıştır. [44]
İZOTOPLAR
Kütle numaraları 250–260 ve 262 olan on iki nobelium izotopu bilinmektedir ve hepsi radyoaktiftir. [50] Ek olarak, nükleer izomerler kütle numaraları 251, 253 ve 254 ile bilinirler. [51] [52] Bunlardan en uzun ömürlü izotop, 58 dakikalık yarı ömür ve en uzun ömürlü 259 Hayır’dır. izomer 1,7 saniyelik yarılanma ömrü ile 251m Hayır’dır. [51] [52] Bununla birlikte, hala keşfedilmemiş 261 No izotopunun 170 dakikalık daha uzun bir yarılanma ömrüne sahip olacağı tahmin edilmektedir. [51] [52] Ek olarak, daha kısa ömürlü 255Bu aktive edilmesinden daha büyük miktarlarda üretildiği için Resim (yarı-ömür 3.1 dakika) genellikle kimyasal deney kullanılır Kaliforniyum-249 ile C–12 iyon. [50] 259 Hayır ve 255 Hayır’dan sonra , sonraki en kararlı nobelium izotopları 253 Hayır (yarı ömür 1,62 dakika), 254 Hayır (51 saniye), 257 Hayır (25 saniye), 256 Hayır (2,91 saniye) ve 252 Hayır (2,57 saniye). [50] [51] [52] Geriye kalan tüm nobelium izotoplarının yarı ömürleri bir saniyeden daha azdır ve en kısa ömürlü bilinen nobelium izotopunun (250 No) yalnızca 0.25 milisaniye yarı ömrü vardır . [50] [51] [52] izotop 254 Hayır bir dizi ortasında olduğu gibi, özellikle teorik ilginç olan yayvan çekirdeklerin 231 Pa kadar 279 Rg ve (iki bilinmektedir ki), nükleer izomerlerinin oluşumu küresel proton kabuğunun hemen üstüne gelen 2f 5/2 gibi proton yörüngeleri tarafından kontrol edilir; 208 reaksiyonunda sentezlenebilir48 Ca ile Pb. [53]
Nobelium izotoplarının yarı ömürleri gelen sorunsuz artış 250 için No 253 dip tarafta görünür, ancak sayılı 254 No ve bunun ötesinde yarılanma ömürleri bile-bile olarak nobelium izotoplar keskin damla kendiliğinden fisyon baskın çürüme modu haline gelir. Örneğin, 256 No’nun yarı ömrü neredeyse üç saniyedir, ancak 258 No’nun yarı ömrü yalnızca 1,2 milisaniyedir. [50] [51] [52] Bu, nobeliumda, protonların karşılıklı itilmesinin, aktinid serisindeki uzun ömürlü çekirdek bölgesi için bir sınır oluşturduğunu göstermektedir. [54] Çift-tek nobelium izotopları, 257 No. [50][51][52] trendindeki düşüşle kütle sayıları arttıkça çoğunlukla daha uzun yarı ömürlere sahip olmaya devam ediyor.
HAZIRLIK VE SAFLAŞTIRMA
Nobelium izotopları, lavrensiyum-262’nin kızı olarak üretilen nobelium-262 haricinde , çoğunlukla aktinid hedeflerin (uranyum , plütonyum , küriyum , kaliforniyum veya einsteinyum) bombardımanıyla üretilir. [50] En yaygın kullanılan izotop olan 255 Hayır, kürium -248 veya kaliforniyum-249’un karbon-12 ile bombardıman edilmesinden üretilebilir : ikinci yöntem daha yaygındır. 350 ışınlanması ug cm -2 üç trilyon (3 x 10 Kaliforniyum-249 hedef 12 ) 73 MeVon dakika boyunca saniyede karbon-12 iyonu yaklaşık 1200 nobelium-255 atom üretebilir. [50]
Nobelium-255 üretildikten sonra, komşu aktinid mendeleviyumun saflaştırılması için kullanılana benzer bir şekilde ayrılabilir. Üretilen nobelium-255 atomlarının geri tepme momentumu, onları üretildikleri hedeften fiziksel olarak uzağa getirmek için kullanılır ve onları hedefin hemen arkasındaki ince bir metal folyoya (genellikle berilyum, alüminyum, platin veya altın) getirir. bir vakumda: bu genellikle nobelium atomlarını bir gaz atmosferinde (genellikle helyum) hapsederek ve reaksiyon odasındaki küçük bir açıklıktan bir gaz jeti ile birlikte taşıyarak birleştirilir. Uzun bir kılcal boru kullanma ve potasyum klorür içeren helyum gazındaki aerosoller, nobelium atomları onlarca metreden fazla taşınabilmektedir. [55] Folyo üzerinde toplanan ince nobelium tabakası, folyoyu tamamen çözmeden seyreltik asit ile çıkarılabilir. [55] Nobelium daha sonra, diğer üç değerlikli aktinitlerin aksine, iki değerlikli durumu oluşturma eğiliminden yararlanılarak izole edilebilir: tipik olarak kullanılan elüsyon koşulları altında ( bis- (2-etilheksil) fosforik asit (HDEHP) sabit organik faz ve 0.05 M mobil sulu faz olarak hidroklorik asit veya katyon değişiminden bir eluant olarak 3 M hidroklorik asit kullanılmasıreçine kolonları), nobelium kolondan geçecek ve diğer üç değerlikli aktinidler kolon üzerinde kalırken ayrılacaktır. [55] Bununla birlikte, doğrudan “yakalayıcı” bir altın folyo kullanılırsa işlem, HDEHP kullanılarak kromatografik ekstraksiyon kolonlarından elüsyon yoluyla nobelium izole edilmeden önce anyon değişim kromatografisi kullanılarak altının ayrılması ihtiyacıyla karmaşıklaşır. [55]
NOTLAR
KAYNAKÇA
KAYNAKLAR
|

